
微信扫一扫
关注公众号
核酸酶残留检测试剂盒,DDM1566A
询价
产品分类
- 酶及底物 (502)
- 免疫学 (3039)
- 标准品/对照品 (528)
- 生物制药与疫苗 (603)
- 分离纯化 (37)
- 生化试剂 (28197)
- 分子生物学 (21)
- WAKO (13228)
- Jackson ImmunoResearch (2012)
- Ludger 糖链分析 (86)
- Lumiprobe活性染料 (3)
- abcam (39004)
- Merck-Sigma (43240)
- MP Bio (10701)
- 试剂 (9464)
- 健康原料 (24)
- 新型材料 (344)
- 仪器分析 (1023)
- 合作品牌 (44303)
- Aalto
- AAT Bioquest
- AbD
- Active Motif
- Advanced Targeting Systems
- Ambion
- AnaSpec
- AssayDesign
- Avanti
- Bangs Laboratories
- BioPorto
- BioSource
- bioworld
- cayman
- Chemicon
- Clontech
- CST
- DiFco
- Epigentek
- hampton
- Himedia
- Hyclone
- ldmsapp
- Innova Biosciences
- Invent
- J.T.BAKER
- KPL
- lifespan
- MRC
- Phytotech
- Pierce
- Prozyme
- Qiagen
- R&D
- Roche
- Santa Cruz
- Vector
- Worthington
- 其他分类 (9)
服务保证
西宝风采
公司新闻
抗体药物生产的质量哨兵-残留检测
发布时间:2025-09-15 10:30 | 点击次数:338
2025年全球抗体工程药物市场规模预计突破3000亿美元,年复合增长率(CAGR)达12%。其中,肿瘤治疗领域占比超60%,自身免疫疾病领域占比约25%,感染性疾病及其他领域占比15%。其中,中国抗体工程药物市场规模预计达1810亿元人民币,年复合增长率达34.58%【1】。在已统计的2024年销售排名前十的药物中过半数为抗体类药物。因此在药物生产放行过程中,如何保证所生产的产品达到放行的合格标准是个关键节点。
表:2024年全球销售额排名前10的药物
|
排名
|
药物名称
|
通用名
|
开发公司
|
2024 年销售额
|
|
1
|
Keytruda(可瑞达)
|
帕博利珠单抗
|
默沙东
|
294.8 亿美元
|
|
2
|
Ozempic(欧唐静)
|
司美格鲁肽
|
诺和诺德
|
169 亿美元
|
|
3
|
Biktarvy(必妥维)
|
比克替拉韦
|
吉利德
|
134 亿美元
|
|
4
|
Eliquis(艾乐妥)
|
阿哌沙班
|
百时美施贵宝、辉瑞
|
133 亿美元
|
|
5
|
Dupixent(达必妥)
|
度普利尤单抗
|
赛诺菲、再生元
|
141.79 亿美元
|
|
6
|
Skyrizi(瑞达珠单抗)
|
利生奇珠单抗
|
艾伯维
|
117.18 亿美元
|
|
7
|
Darzalex(兆珂)
|
达雷妥尤单抗
|
强生
|
116.7 亿美元
|
|
8
|
Stelara(喜达诺)
|
乌司奴单抗
|
强生
|
103.6 亿美元
|
|
9
|
Humira(修美乐)
|
阿达木单抗
|
艾伯维
|
89.9 亿美元
|
|
10
|
Opdivo(欧狄沃)
|
纳武利尤单抗
|
百时美施贵宝
|
93.04 亿美元
|
1、CHO宿主细胞残留DNA检测试剂盒
CHO细胞是生物制药行业应用最广泛的细胞系。在药物表达生产过程中,不可避免的会有一些来自于宿主细胞核酸的残留,药典推荐的外源性DNA残留检测方法有DNA探针杂交法、荧光染料染色法和定量PCR法。目前,荧光探针qPCR法是主流HCD检测手段,因高灵敏度、序列特异性及准确性,为生物制药工艺研究和质量控制提供可靠数据。
本试剂盒采用qPCR荧光探针法原理,与宿主细胞残留DNA提取试剂盒搭配使用可快速高效的定量检测各类生物制品及药品的中间品、半成品和成品中残留的CHO宿主细胞DNA。检测快速、特异性强、检测灵敏度高,最低检测限可以达到fg级。
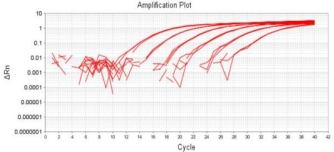
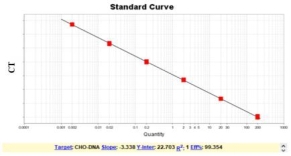
线性范围为:0.002pg/μL-200pg/μL;复孔差异小,扩增效率高,检测值偏差<15%
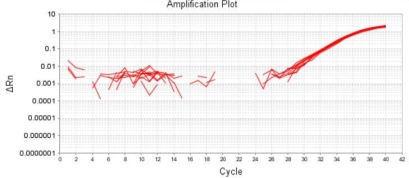
经过灵敏度测试,本试剂盒定量限可达1fg/μL,具有高灵敏度。
2、CHO细胞残留蛋白检测试剂盒
CHO细胞宿主细胞的蛋白残留,这些残留的宿主细胞蛋白会降低药物的疗效,而且会有很大的潜在风险,在进入人体后可能会诱发严重的不良反应;因此,需要对生物药物中的宿主细胞残留蛋白进行严格检测。美国药典(USP<1132>)规定HCP残留应<100ppm(即1mg总蛋白中HCP含量<100ng,<0.01%);欧洲药典(EP2.6.34)规定HCP残留应<0.1%(1000ppm);中国药典规定CHO细胞:HCP残留需<0.05%(500ppm),推荐的检测方法有ELISA法和免疫印迹法,其他补充方法液相色谱-质谱联用(LC-MS/MS)法
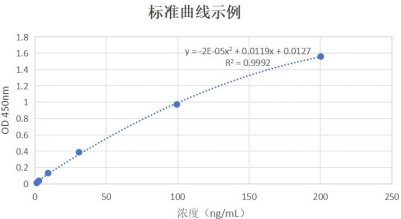
检测灵敏度为:1ng/mL,线性范围为:1ng/mL-200ng/mL
3、鼠细小病毒(MMV)检测试剂盒
生物制药领域源细胞如CHO、NS0及BHK-21等细胞是广泛应用的工程细胞,此类细胞容易发生鼠细小病毒(MouseMinuteVirus,以下简称MMV)污染。MMV具有极强的稳定性,不易清除和灭活,有更高的安全风险,前已经成为危害生物制品安全的一个重要因素。我司提供的鼠细小病毒(MMV)检测试剂盒,采用qPCR荧光探针法原理,与病毒核酸提取试剂盒搭配使用使用,可快速高效的定性检测各类生物制品中鼠细小病毒(MMV)的污染。
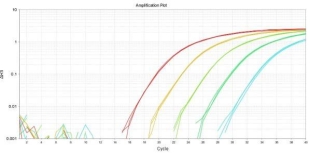
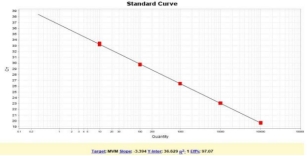
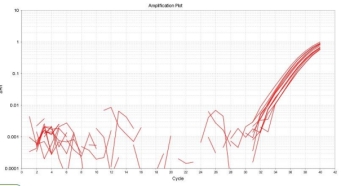
经梯度稀释MMV质粒参考品测试,基因组拷贝数在105—10copies/μL时,本产品的R2=1,扩增效率97.07%
4、宿主细胞残留DNA提取试剂盒(磁珠法)
本试剂盒用于生物制品样本的前处理,可稳定高效地获得样本中的微量宿主细胞DNA。适用于多种基质缓冲溶液,有效提取纯化微量的DNA。本试剂盒可搭配HCD检测试剂盒共同使用,可快速高效的定量检测各类生物制品中来自宿主细胞的残留DNA。
1、除了手动提取试剂盒,还有与全自动核酸提取仪配套的自动化提取试剂盒,供不同需要的客户选择使用。
2、提取高效快速(自动化版本仅需26min),提取效率高。
3、针对不同类型的样本,回收率在80%-120%之间,且重复性好。
【1】中研普华产业研究院《2025-2030年中国抗体工程药物行业市场深度调研及投资策略预测报告》
相关产品
|
产品名称
|
规格
|
|
CHO细胞残留蛋白检测试剂盒
|
96T
|
|
蛋白A(ProteinA)残留检测试剂盒
|
48/96T
|
|
宿主细胞残留DNA提取试剂盒
|
100reaction/盒
|
|
CHO宿主细胞残留DNA检测试剂盒
|
100reaction/盒
|
|
E.coli宿主DNA残留检测试剂盒
|
100reaction/盒
|
|
毕赤酵母残留DNA检测试剂盒
|
100reaction/盒
|
|
Vero残留DNA检测试剂盒
|
100reaction/盒
|
|
HEK293细胞残留DNA检测试剂盒
|
100reaction/盒
|
|
SV40LTA&E1A残留DNA检测试剂盒
|
100reaction/盒
|
|
质粒DNA残留检测试剂盒
|
100reaction/盒
|
|
支原体DNA提取纯化试剂盒
|
50reaction/盒
|
|
支原体Qpcr检测试剂盒
|
100reaction/盒
|
|
病毒核酸提取试剂盒
|
50reaction/盒
|
|
RCL基因拷贝数检测试剂盒
|
100reaction/盒
|
|
鼠细小病毒(MMV)检测试剂盒
|
50T
|
|
细菌DNA检测试剂盒
|
20T/50T
|
|
真菌DNA检测试剂盒
|
20T/50T
|


















