
微信扫一扫
关注公众号
COLLAGEN TYPE IVMONOCLONAL ANTIBODY
询价
产品分类
- 酶及底物 (520)
- 免疫学 (3087)
- 标准品/对照品 (536)
- 生物制药与疫苗 (604)
- 分离纯化 (37)
- 生化试剂 (28748)
- 分子生物学 (21)
- WAKO (13608)
- Jackson ImmunoResearch (2012)
- Ludger 糖链分析 (87)
- Lumiprobe活性染料 (3)
- abcam (39100)
- Merck-Sigma (44401)
- MP Bio (11006)
- 试剂 (9706)
- 健康原料 (24)
- 新型材料 (345)
- 仪器分析 (1025)
- 合作品牌 (44464)
- Aalto
- AAT Bioquest
- AbD
- Active Motif
- Advanced Targeting Systems
- Ambion
- AnaSpec
- AssayDesign
- Avanti
- Bangs Laboratories
- BioPorto
- BioSource
- bioworld
- cayman
- Chemicon
- Clontech
- CST
- DiFco
- Epigentek
- hampton
- Himedia
- Hyclone
- ldmsapp
- Innova Biosciences
- Invent
- J.T.BAKER
- KPL
- lifespan
- MRC
- Phytotech
- Pierce
- Prozyme
- Qiagen
- R&D
- Roche
- Santa Cruz
- Vector
- Worthington
- 其他分类 (9)
服务保证
西宝风采
公司新闻
I型胶原蛋白(Collagen, CAS:9007-34-5)
发布时间:2023-12-11 09:03 | 点击次数:3402
胶原蛋白(Collagen)是人体中非常重要的一种蛋白质,主要是由成纤维细胞或其他类似的细胞,比如成骨细胞和成软骨细胞产生的。在所有胶原蛋白中,I型胶原蛋白是最为人所知且分布最广泛的类型。它不仅是皮肤、骨骼、肌腱等纤维结缔组织的主要结构性成分,还在分子结构上与其他类型的胶原蛋白有明显的不同。
I型胶原蛋白的结构特点是由两条α1链和一条α2链组成的异源三聚体,每条链都含有超过1000个氨基酸。这三个多肽链以三螺旋的形式存在,这是由胶原蛋白的一级结构决定的。在一级结构中,氨基酸序列呈现出重复的基序,通常每三个氨基酸就会包括甘氨酸、脯氨酸或者甘氨酸残基前的4-羟基脯氨酸。I型胶原蛋白在中性环境下能自发形成三螺旋支架,这种结构对于维持皮肤的弹性、骨骼的强度以及肌腱的韧性等都至关重要。
产品特点:
提取的高质量纯化蛋白
高水平自交联
建议使用高粘度溶液专用移液器
低自发荧光
高度标准化的制造流程和严格的质量控制
高水平自交联
建议使用高粘度溶液专用移液器
低自发荧光
高度标准化的制造流程和严格的质量控制
I型胶原蛋白产品
|
产品来源
|
包装规格
|
胶原含量
|
外观性状
|
纯度
|
分子量
|
|
牛筋腱
|
5g/100g (粉)
|
>85%
|
白色至浅黄色,均匀粉末或颗粒,无结块。
|
≥96%
|
约300kDa
|
|
牛筋腱
|
1kg/5kg (液体)
|
7mg/ml
|
澄清或呈乳白色的半透明,具有一定粘度的液体。
|
≥96%
|
约300kDa
|
详询西宝生物产品,请咨询:400-021-8158 / 021-50272975。
I型胶原蛋白作为一种科研试剂,具有广泛的应用价值,尤其在细胞学、药理学等科研领域。由于其对人体可能产生不良影响,因此严禁将其用于人体。在科研实验中,I型胶原蛋白在细胞生长、分化、迁移以及组织形态的发生等过程中发挥着重要作用。为了确保实验效果,合理使用I型胶原蛋白非常重要。
胶原蛋白支架融入全层皮肤伤口:连接蛋白反应
胶原蛋白支架被用于促进全层皮肤伤口的愈合,特别是在难以愈合的伤口,如烧伤和慢性溃疡。研究评估了胶原蛋白支架对小鼠全层伤口在愈合初始阶段(前5天)的再上皮化的影响。结果显示,胶原蛋白支架抑制了伤口的正常上皮再生过程,导致了伤口边缘的表皮增厚,而不是正常愈合过程中观察到的角质形成细胞的迁移。
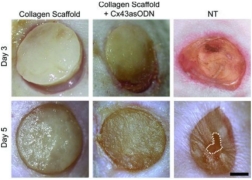
(在伤口形成后的第3天和第5天,对伤口进行了宏观摄影。照片中,虚线标出了再上皮化的可见前沿,展示了所有小鼠(n = 7)的典型情况,比例尺=1.5毫米)
胶原蛋白 I 和胶原蛋白 III 在组织损伤和再生中的调节
在皮肤损伤愈合过程中,胶原纤维的分布会发生改变,胶原I和胶原III的比例也会随之变化。在愈合过程中,胶原I的增加和胶原III的减少是瘢痕成熟和伤口强化的标志。
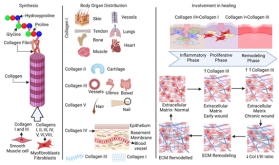
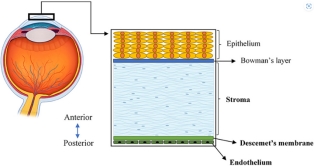
胶原蛋白I型和胶原蛋白IV型在制备透明眼部组织方面的应用
胶原蛋白的多样化组织结构是其形态可塑性的关键因素。其在形成多种组织类型方面的重要性推动了胶原蛋白作为生物材料的研发和应用。角膜和晶状体组织中主要存在胶原蛋白I型(Col-I)和胶原蛋白IV型(Col-IV),这两种胶原蛋白对于组织结构的稳定性和透明度至关重要,保证了视觉的清晰。回顾了这两种胶原蛋白作为生物工程新型生物材料在制备独特组织中的应用,这些组织有可能用于治疗导致失明的多种眼科疾病。
胶原蛋白I 型作为骨组织工程的支架生物材料
胶原蛋白I型(Col-I)是构成骨细胞外基质的主要有机成分,常用作骨组织工程中的支架材料。聚合物胶原蛋白易于从多种动物来源提取,并能通过多种工艺加工成不同形态的生物材料,如海绵、颗粒或水凝胶,以适应多种应用场景。尽管胶原蛋白I型具有良好的生物相容性和引导骨生长的能力,但它也存在一些局限,例如易被生物降解、机械强度不足以及缺乏骨诱导性。因此,研究者们致力于通过各种方法提升基于胶原蛋白I型的骨植入物的性能。
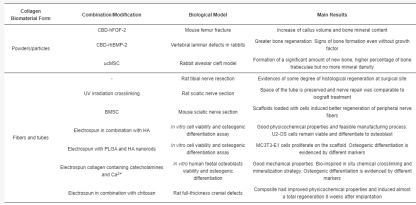
CBD-FGF-2(胶原蛋白结合域-成纤维细胞生长因子2);ucMSC(脐带来源的间充质干细胞);PLGA(聚乳酸-羟基乙酸共聚物);BMP(骨形态发生蛋白)
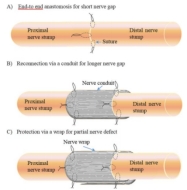
胶原蛋白I 型:一种多功能生物材料
在神经缺损修复中,根据缺损的类型,治疗方法也会有所不同。对于短神经间隙,可以采用直接端端吻合的方法进行修复。而对于神经间隙在0.5厘米至6厘米范围内的横断神经,则可能需要使用自体移植物或神经导管。此外,对于部分缺损或压碎的神经,通常采用神经包裹技术来保护神经,以促进神经再生。
胶原蛋白生物材料作为药物递送系统
在药物递送领域,胶原蛋白作为一种生物材料,因其高载药能力、良好的生物相容性和生物可降解性,已被广泛研究和应用。然而,胶原蛋白基药物递送系统(CDSS)在临床试验中仍面临许多挑战,特别是在细胞内分子(如基因)的递送方面。为了应对这些挑战,可以通过实验结果、理论模型和分子模拟来优化CDSS的设计和制造,从而提高对特定治疗靶点的精准控制递送,并进一步理解其治疗机制。此外,胶原蛋白的模块化特性使其成为构建个性化药物递送系统的理想选择,这些系统可以根据患者的具体需求和疾病情况量身定制。

用于药物递送的不同类型胶原蛋白基生物材料
|
Collagen/ collagen composite
|
Drug/active substance
|
Medicinal application
|
|
Collagen
|
Keterolac
|
Inflammation
|
|
Collagen
|
TA
|
Drug release and kinetics
|
|
Collagen
|
NGF-β
|
Sustained delivery and corneal regeneration
|
|
Collagen
|
Apis mellifera royal jelly
|
Delivery vehicle for wound healing
|
|
Collagen
|
Curcumin
|
Controlled anti- proteolytic and pro-angiogenic efficacy
|
|
Gelatin
|
Essential oil of Eupatorium adenophorum
|
Antibacterial wound dressing
|
|
Collagen/ ALG
|
BSA
|
Ocular drug delivery
|
|
Collagen/ ALG
|
—
|
Cell proliferation
|
|
Collagen/ HEMA
|
GA, naproxen
|
Drug release, antimicrobial potential
|
|
Collagen/ Fe3O4 NPs
|
Fluorescein
|
Delivery, release and cell viability
|
|
Collagen/ CHS
|
QHREDGS
|
Myocardial infarction
|
|
Gelatin/ CHS/ ALG
|
5-FU
|
Anti cancer drug delivery
|
|
Collagen/ ALG
|
Methylene blue imiquimod
|
Combinatorial photothermal and immune tumor therapy
|
|
Collagen/ CHS
|
Tumor necrosis factor-α (TNF- α)
|
Drug delivery and tissue filler
|
|
Collagen/ graphene oxide (GO)
|
FGF-2
|
Controlled release
|
参考文献:
[1]. Daniel J. Gilmartin, et al. Integration of Scaffolds into Full-Thickness Skin Wounds: The Connexin Response. doi.org/10.1002/adhm.201200357
[2]. Drishtant Singh, et al. Regulation of Collagen I and Collagen III in Tissue Injury and Regeneration. doi: 10.26502/fccm.92920302
[3]. Yihui Song, et al. Application of Collagen I and IV in Bioengineering Transparent Ocular Tissues. doi.org/10.3389/fsurg.2021.639500
[4]. Gustavo A. Rico-Llanos, et al. Collagen Type I Biomaterials as Scaffolds for Bone Tissue Engineering. doi.org/10.3390/polym13040599
[5]. Amit Kumar Verma, et al. Collagen-Based Biomaterial as Drug Delivery Module. DOI: 10.5772/intechopen.103063


















